
TRIBUNES
Greffes osseuses
Matériaux de comblement osseux
Greffes autologues
Allogreffes et biomatériaux
GREFFE OSSEUSE
GREFFES OSSEUSES AUTOLOGUES, ALLOGREFFES ET BIOMATERIAUX
Par le Dr. L. BENSLAMA
Chirurgien stomatologiste et maxillo-facial. Praticien de l’hôpital de la Pitié-Salpêtrière et de l’hôpital Américain de Paris.
69, rue de la Tour, 75016 Paris.
Editorial
Rev. Stomatol. Chir. Maxillofac., 2005 ; 106, 3, 133-135
© Masson, Paris, 2005
DÉSERT SCIENTIFIQUE
Il y a quelques jours, sur le forum de discussion de l'Association Française des Jeunes Chirurgiens Maxillo-Faciaux (AFJCMF)[1] , un des membres a lancé un appel. Le voici : "J'aimerai savoir si quelqu'un connaît un article de vulgarisation expliquant que le meilleur matériel de comblement reste l'os autologue et non pas les biomatériaux, car j'ai un patient qui veut absolument voir un article ; car un chirurgien dentiste lui propose une greffe allogénique, et moi, bien évidemment, une prise de pariétal. Merci de votre aide... "
Interpellé par cet appel, soir après soir, en vain, j'ai guetté les réponses de la part de ceux qui, nombreux et parfois maîtres de la discipline, fréquentent ce forum. Seules trois réponses ont été données :
- la première renvoyait à un livre, plutôt très spécialisé, de JF Tulasne,
-
la seconde à une publication en cours du même auteur,
- la troisième rapportait comme une rumeur, que tel ou tel praticien, dentiste, en Allemagne, au Canada, aux Etats Unis, pratiquait des greffes allogéniques au cabinet, sous anesthésie locale, avec de "bons résultats".
Force est de constater que dans ce domaine les informations fiables manquent, et qu'une revue de la littérature montre l'absence de toute étude scientifique prospective comparative, prenant l'os autogène comme matériau de référence. De nombreuses publications rapportent quelques cas cliniques, mais leur valeur scientifique reste médiocre, principalement en raison du faible nombre de sujets concernés ou de l'absence de recul suffisant. Dans les congrès et les publications, la quasi totalité des grands services hospitalo-universitaires en sont encore à rapporter leur expérience des autogreffes, laissant de côté ou occultant les autres matériaux. Ce "désert" scientifique est d'autant plus étonnant que l'on sait que l'utilisation d'os humain de banque ou d'hydroxy-apatite bovine par exemple, est une pratique quotidienne de nombreux acteurs de santé. Il serait inconscient de l'ignorer.
RELANCER LE DÉBAT
Il m’a semblé opportun de relancer le débat et de tenter une mise au point sur cette question : quelle place pour les greffes osseuses allogéniques et pour les "biomatériaux" en chirurgie maxillo-faciale, et plus particulièrement en chirurgie pré-implantaire, domaine où les chirurgiens dentistes sont de plus en plus présents et où ils se métamorphosent en de véritables concurrents, là où l’on attendait des correspondants potentiels ?
Il est inutile de revenir sur les raisons qui amènent à rechercher une alternative aux autogreffes, quel qu’en soit le site de prélèvement. Pour simplifier, rappelons ce que Paul Tessier, qui en pratiqua plus de neuf mille (9000) écrivait dans un commentaire d’article [2] : pour le patient, c’est un handicap souvent douloureux. Pour le chirurgien c’est du temps passé, dit "temps perdu".
Le principal argument très tôt opposé à l’utilisation des allogreffes et des biomatériaux en chirurgie pré-implantaire est l’absence d’ostéoconduction et/ou d’ostéo-induction. La conviction était que ces matériaux, tolérés par l’organisme, n’impliquaient nullement qu’ils puissent se transformer en os vivant vascularisé pour que l’ostéo-intégration se fasse et persiste. Pour certains matériaux, tel le corail, on craignait l’apparence de la continuité et l’interposition, ce qui est vraisemblable. Pour d’autres matériaux, ce qui était redouté, c’était la calcification plutôt que l’ossification. Ceci est également vraisemblable pour les blocs d’allogreffes totales réfrigérées, lyophyilisées, donnant "des os morts pseudarthrosés, des os feuilletés inconsistants"[4]
Depuis, de nombreux travaux ont prouvé qu’un véritable processus d’ossification, impliquant résorption ostéoclastique et régénération ostéoblastique était possible avec certains matériaux, plus particulièrement l’os humain de banque lyophylisé déminéralisé ou non [3] et [4]. Les taux de succès implantaire dans les séries rapportées sont comparables à ceux des implants placés dans les autogreffes ou dans l’os non greffé. Lors de la conférence de consensus de Boston en 1996 les rapporteurs écrivent dans leurs conclusions : "les taux de survie des implants étant remarquablement similaires et du fait de la multiplicité des variables, il est impossible d’affirmer avec certitude qu’un matériau est meilleur qu’un autre" [5]. Ces résultats étant acquis et le débat clos depuis longtemps pour nombre d’intervenants, les travaux portent actuellement plutôt sur l’optimisation des indications : "quel matériau pour un comblement de sinus ?", "quel autre pour une greffe d’apposition verticale ou horizontale ?", etc. Par ailleurs, l’utilité de l’association à de l’os autologue ou de l’incorporation de facteurs de croissance osseuse du type palatal rich fibrin (PRF®) pour accélérer les processus de ré-ossification fait l’objet de multiples essais.
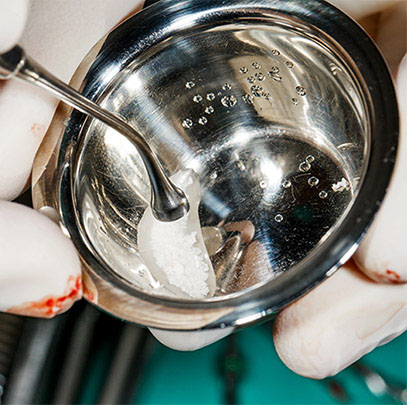
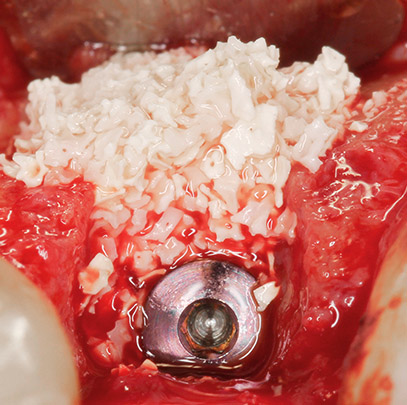
Dans notre expérience au service de Stomatologie et de Chirurgie Maxillo-Faciale de l’hôpital Tenon (Dr J. Lalo, Paris) et à l’Hôpital Farhat Hached (Pr C. Baccouche, Sousse, Tunisie), ces résultats se vérifient avec un recul supérieur à 6 ans pour l’utilisation d’os humain de banque lyophylisé non minéralisé (os Phoenix®, laboratoires TBF), seul ou associé à l’os autogène. Nous avons déjà rapporté l’intérêt que nous avions pour l’os broyé. [6] Cette présentation sous forme de copeaux d’os autologue, de poudre d’os spongieux de granulométrie variant de 0,2 à 0,8 mm ou de lamelles nous semble, avec le recul, d’importance. Notre conviction est que les fragments de petite taille, inondés par le sang et ses apports en cellules mésenchymateuses permettent une ostéo-induction et une ostéoconduction en des dizaines de milliers d’endroits, au contraire d’un fragment disposé en bloc d’une certaine taille. Celui-ci s’interposerait et gênerait la diffusion en de multiples points des cellules apportées par le sang. Plus que le matériau lui-même, c’est le sang et ses apports qui nous semblent importer dans le processus de reconstruction osseuse. Tout récemment, une équipe américaine est venue démontrer pour la première fois la présence en quantité physiologiquement significative d’ostéoblastes dans la circulation sanguine. [7] Ces cellules représentent un capital probablement mis en jeu dans la régénération des défects osseux, et dans le processus de réossification tel que nous le connaissons depuis de nombreuses années. Nul besoin de migration des ostéocytes et ostéoblastes à partir de l’os adjacent ou en place, ils sont dans le sang qui inonde le site.
Ainsi s’expliqueraient d’une part les résultats comparables obtenus en chirurgie osseuse pré-implantaire indépendamment du matériau utilisé, d’autre part, l’efficience de la régénération osseuse guidée, l’ossification des hématomes et bien d’autres phénomènes. Quel que soit le « dispositif » présent - os, biomatériau, périoste, membrane titane - celui-ci joue le rôle de " conformateur d’espace", de " mainteneur de volume", séparant l’os adjacent des muqueuses, permettant au sang et à ses cellules mésenchymateuses d’occuper cet espace et d’y entamer le processus d’ostéo-induction, d’ostéoconduction, de résorption éventuelle du matériau en place et de son remplacement par de l’os néoformé. Il va de soit que « l’étanchéité » de ce volume par rapport aux cellules épithéliales muqueuses ou conjonctives est une condition nécessaire. Celles-ci sont en effet toujours gagnantes devant les cellules osseuses dans la course pour occuper l’espace si elles en avaient la possibilité.
Notre point de vue, celui de la « primeur du sang sur le matériau », s’il était confirmé, modifierait radicalement notre conception et nos approches de la reconstruction osseuse. Il nous permet déjà dans notre équipe de faire souvent le choix de l’os autologue broyé plutôt que des blocs, ainsi que celui, de plus en plus fréquent, de la poudre ou des lamelles d’os humain lyophilisé non déminéralisé. Ce matériau est susceptible d’être complètement résorbé pour être remplacé par de l’os néoformé, contrairement à l’hydroxy-apatite ou aux bio-verres dont la résorption est partielle ou nulle.
RÉGLEMENTATIONS DRACONIENNES EN FRANCE
Un autre argument est souvent opposé à l’utilisation d’os humain de banque, celui du risque immunogène ou de transmission à l’homme de maladies par des agents d’origine animale telles que la variante de la maladie de Creutzfeldt-Jakob (v-MCJ)
Rappelons d’abord qu’en raison d’affaires largement médiatisées, (sang contaminé, hormone de croissance), l’Europe et plus particulièrement la France se sont dotées de réglementations draconiennes en la matière. Le statut "banque de tissus", accordé à une quarantaine d’entreprises publiques et à quelques autres privées, est d’une extrême rigueur. Il est régi par de multiples décrets : les bonnes pratiques, le décret banque, les lois de bio-éthique etc. Les autorisations sont données pour cinq ans. Les établissements assurent la collecte, la transformation et la distribution de têtes fémorales prélevées sur des donneurs vivants sélectionnés cliniquement et biologiquement lors d'une arthroplastie de hanche. Le recueil est réalisé par des chirurgiens orthopédistes dans des établissements de santé français, et ce dans le respect des lois dites de bioéthique. Les procédés de transformations spécifiques conduisent à un matériau de comblement dévitalisé, lyophilisé et radiostérilisé, pouvant être conservé à température ambiante. La distribution obéit à des règles strictes d’information et de traçabilité.
Les processus de préparation de l’os humain de banque, en particulier l’inactivation virale, éliminent certains risques, mais pas complètement celui de la v-MJC. C’est ce point qui est mis en avant pour justifier le recours aux seules greffes autologues (principe de précaution). Le risque de transmission de la variante de la v-MCJ par le sang et ses dérivés, a fait l’objet d’un examen annuel par un groupe d’experts multidisciplinaire et indépendant depuis 2000. [8] La lecture de ces rapports donne la mesure de ce risque pour les tissus greffés. On y lit : "Enfin, il est rappelé qu’aucun cas de transmission à l’homme de la v-MCJ par des greffons n’a été signalé en France par la biovigilance… La présence d’une éventuelle infectiosité dans les greffons est fonction de la répartition de l’infectiosité de la v-MCJ, supposée être circonscrite à un nombre limité d’organes et de tissus (cerveau, rétine, nerf optique, formations lymphoïdes secondaires i.e. amygdales, rate, ganglions lymphatiques), de surcroît non concernés par la greffe… Pour ce qui est des greffons prélevés en France, le risque de contamination peut être estimé comme étant comparable à celui des produits sanguins labiles, soit pour le receveur un risque de 1 sur 120 000 par greffon… Cette approche est peut-être conservatoire pour des greffons peu vascularisés et renfermant peu ou pas de cellules du système réticulo-endothélial".
Ainsi donc, de l’aveux même des experts, le calcul du risque et les mesures préconisées sont "conservatoires" pour des greffons peu vascularisés, ce qui est le cas de l’os humain déprotéïnisé, lyophylisé, ayant subi de multiples procédés d’inactivation virale et biochimique. Autrement dit, c’est bien le "principe de précaution" qui est mis en avant, principe tout récemment inscrit dans la constitution (article 5) selon un consensus politique et social très large. Les récentes catastrophes que le pays a connues, comme l’amiante, le sang contaminé, les farines animales et la canicule y sont certainement pour quelque chose, mais dans chacun de ces cas des indices avant-coureurs qui auraient pu être pris en compte à temps, ne l’ont pas été. Parce que ces indices n’ont pas été jugés probants ou parce que des intérêts économiques sont passés devant, ou par simple laxisme.
On est loin de cette situation en matière d’allogreffes, et l’application du principe de précaution y frôle l’absurde. Certains semblent l’avoir compris. D’ailleurs, d’autres situations et activités, comme l’alcool, le tabac ou la voiture, montrent les limites, l’ambiguité, voire la contradiction de ce principe de précaution. Dans ces cas, le plaisir et le besoin peuvent être mis en premier plan. Le principe de précaution fait l’unanimité pour le sang contaminé, il ne le fait pas pour la cigarette.
Même inscrit dans la constitution, le principe de précaution ne doit pas être appliqué aveuglément. Un tel principe de précaution qui freinerait la science et l’expérimentation, au nom d’un bien-être naïf, appliqué dans le passé, nous aurait privés de quasiment tout ce dont nous disposons aujourd’hui.
Il est temps d’ouvrir le débat dans notre discipline, car il ne faut pas que la recherche institutionnelle, particulièrement celle des grands services hospitaliers français en pâtisse : nous risquerions de devoir payer le prix fort pour ce que les autres auront eu la "folie" de mettre au point.
1
AFJCMF@yahoogroupes.fr
2
A propos de l’article : greffe osseuse du sinus maxillaire et implants Branemark (J-F Tulasne, J. Saade, A. Riachi). Implants 1993 ; 2 : 209-213
3
Van der Bergh J.P., Ten Bruggenkate C. M et al. Maxillary sinus floor elevation with human demineralized freeze dried bone. Clin. Oral Impl. Res 2000 : 3 ; 209-214
4
Piattelli A, Scarano A, Piattelli M. Microscopic and histochemical evaluation of demineralized freeze-dried bone allograft in association with implant placement: a case report. Int J Periodontics Restorative Dent. 1998 Aug;18(4):355-61.
5
Jensen O.T., Shulman L. B., Block M. S., Iacono V. J. Report of the sinus consensus confernece of 1996. Int. J. of Oral and Maxillofac. Impl. 1998 ; 13 (supplement)
6
J. Lalo, L. Ben Slama, M. Djemil, G. Aractingi, G. Boukhris, J.P. Casteyde. Comblement osseux sous sinusien : intérêt de l’utilisation d’os cortical broyé Rev Stom Chir Max fac. 2003.104 ; 2 :
7
Eghbali-Fatourechi G. Z., Lamsam J., Fraser D., Nagel D., Riggs B. L., Khosla S. Circulating Osteoblast-Lineage Cells in Humans N Engl J Med 2005; 352:1959-1966
8
AFSSAPS. Analyse du risque de transmission de la variante de la maladie de Creutzfeld-Jakob par les produits de santé et par les tissus et fluides d’origine humaine. Rapports : décembre 2000, février 2002, mars 2003, février 2004.
